Soal Olimpiade Kimia OSN-K SMA 2016

AYO BERLATIH
Soal Olimpiade Kimia OSN-K SMA 2016
| Nama Peserta | : | |
| Tanggal Test | : | |
| Jumlah Soal | : | 30 soal |
| Waktu | : | 90 menit |
Pilihlah Jawaban yang tepat.
1. Larutan kalium permanganat direaksikan dengan kalium oksalat dalam suasana basa menghasilkan mangan oksida ($\text{MnO}_2$) dan karbondioksida. Maka koefisien kalium permanganat dan kalium oksalat setelah reaksi setara yaitu:
A. 4 dan 2
B. 2 dan 3
C. 3 dan 2
D. 2 dan 6
E. 4 dan 8
2. Di antara larutan aqueous pada pilihan A, B, C, D dan E berikut, larutan aqueous yang dapat bereaksi dengan logam magnesium adalah:
A. Ammonia, $\text{NH}_3$
B. Kalium hidroksida,KOH
C. Hidrogen chlorida, HCl
D. Natrium hidrogencarbonat
E. Semua larutan di atas (pada pilihan A, B, C dan D) dapat bereaksi dengan Mg
3. Bila gelembung gelembung gas chlorin dialirkan kedalam larutan natrium hidroksida pekat panas, akan terbentuk larutan:
A. NaCl dan NaClO
B. NaCl dan $\text{NaClO}_3$
C. NaClO dan $\text{NaClO}_3$
D. NaClO saja
E. $\text{NaClO}_3$ saja
4. Reaksi berikut ini, manakah yang merupakan reaksi redoks?
a. $\text{K}_2\text{CrO}_4(aq)+\text{BaCl}_2(aq)$ $\to $ $\text{BaCrO}_4+2\text{KCl}(aq)$
b. $\text{Na}(s)+\text{H}_2\text{O}(l)$ $\to $ $\text{NaOH}+\text{H}_2(g)$
c. $\text{Pb}^{2+}(aq)+2\text{Br}^-(aq)$ $\to $ $\text{PbBr}_2(s)$
d. $\text{Cu}(s)+\text{S}(s)\to \text{CuS}$
a. $\text{K}_2\text{CrO}_4(aq)+\text{BaCl}_2(aq)$ $\to $ $\text{BaCrO}_4+2\text{KCl}(aq)$
b. $\text{Na}(s)+\text{H}_2\text{O}(l)$ $\to $ $\text{NaOH}+\text{H}_2(g)$
c. $\text{Pb}^{2+}(aq)+2\text{Br}^-(aq)$ $\to $ $\text{PbBr}_2(s)$
d. $\text{Cu}(s)+\text{S}(s)\to \text{CuS}$
A. Hanya a dan c
B. Hanya a, b dan c
C. Hanya b, c dan d
D. Hanya b dan d
E. semuanya adalah reaksi redoks
5. Setengah reaksi yang terjadi di anoda dalam persamaan berikut:
$3\text{MnO}_4^-(aq)+24\text{H}^+(aq)+5\text{Fe}(s)$ $\to $ $3\text{Mn}^{+2}(aq)+5\text{Fe}^{+3}(aq)+12\text{H}_2\text{O}(l)$ adalah
$3\text{MnO}_4^-(aq)+24\text{H}^+(aq)+5\text{Fe}(s)$ $\to $ $3\text{Mn}^{+2}(aq)+5\text{Fe}^{+3}(aq)+12\text{H}_2\text{O}(l)$ adalah
A. $\text{Fe}^{+2}(aq)\to \text{Fe}^{+3}(aq)+\text{e}^-$
B. $\text{MnO}_4^-(aq)+8\text{H}^+(aq)+5\text{e}^-$ $\to $ $\text{Mn}^{+2}(aq)+4\text{H}_2\text{O}(l)$
C. $\text{Fe}(s)\to \text{Fe}^{+3}(aq)+3\text{e}^-$
D. $2\text{MnO}_4^-(aq)+12\text{H}^+(aq)+6\text{e}^-$ $\to $ $2\text{Mn}^{+2}(aq)+3\text{H}_2\text{O}(l)$
E. $\text{Fe}(s)\to \text{Fe}^{+2}(aq)+2\text{e}^-$
6. Sebanyak 2 gram sampel gas hidrogen ($_1^1\text{H}$ ) pada temperatur T dan volume V memberikan tekanan P. Gas deuterium, $_1^2\text{H}$, adalah suatu isotop dari hidrogen. Berikut ini, kondisi manakah yang juga akan memberikan tekanan sebesar P pada temperatur T yang sama?
A. 2 g deuterium volume V
B. 4 g deuterium volume V/2
C. Campuran 1 g hidrogen dan 2 g deuterium dengan total volume V
D. Campuran 2 g hidrogen dan 1 g deuterium dengan total volume 2V
E. Campuran 2 g hidrogen dan 2 g deuterium dengan total volume 2V
7. Berikut ini adalah alur nilai PV/RT terhadap P, untuk gas ideal dan gas non-ideal.
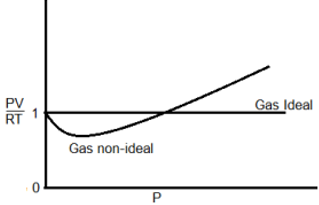
P adalah tekanan gas, V adalah volume gas, R adalah tetapan gas ideal dan T adalah temperatur. Dari gas gas berikut ini, manakah yang menunjukkan deviasi (penyimpangan) paling besar dari sifat gas ideal?

P adalah tekanan gas, V adalah volume gas, R adalah tetapan gas ideal dan T adalah temperatur. Dari gas gas berikut ini, manakah yang menunjukkan deviasi (penyimpangan) paling besar dari sifat gas ideal?
A. Helium
B. Nitrogen
C. Metana
D. Etena
E. Ammonia
8. Diantara senyawa berikut ini, manakah yang mempunyai tekanan uap paling rendah:
A. Air, $\text{H}_2\text{O}$
B. Hidrogenperoksida, $\text{H}_2\text{O}_2$
C. Etanol, $\text{CH}_3\text{CH}_2\text{OH}$
D. Aseton, $\text{CH}_2\text{CO}-\text{CH}_2$
E. Asam asetat, $\text{CH}_3\text{COOH}$
9. Dibandingkan dengan air murni, larutan NaCl 0,1 mol/L mempunyai:
A. pH lebih tinggi
B. Daya hantar listrik lebih rendah
C. Titik didih lebih rendah
D. Titik beku lebih rendah
E. Tekanan uap lebih tinggi
10. Perhatikanlah unsur unsur dalam susunan berkala yang terdapat dalam perioda ke 2 dari blok-$p$. Energi ionisasi pertama dari unsur unsur ini adalah:
A. Naik dari B ke Ne
B. Turun dari B ke Ne
C. Naik dari B ke O, turun untuk F, dan kemudian naik untuk Ne
D. Turun dari B ke N dan naik beraturan dari N ke Ne
E. Naik dari B ke N, turun untuk O dan naik dari O ke Ne
11. Berikut ini mengenai radius ion, berturut turut: $\text{F}^-$, $\text{N}^{-3}$, $\text{P}^{-3}$, $\text{S}^{-2}$. Urut urutan yang benar mengenai radius ion tersebut adalah:
A. Radius $\text{F}^-$ > $\text{N}^{-3}$ > $\text{P}^{-3}$ > $\text{S}^{-2}$
B. Radius $\text{S}^{-2}$ > $\text{P}^{-3}$ > $\text{N}^{-3}$ > $\text{F}^-$
C. Radius $\text{P}^{-3}$ > $\text{N}^{-3}$ > $\text{S}^{-2}$ > $\text{F}^-$
D. Radius $\text{P}^{-3}$ > $\text{S}^{-2}$ > $\text{N}^{-3}$ > $\text{F}^-$
E. Radius $\text{N}^{-3}$ > $\text{S}^{-2}$ > $\text{F}^-$ > $\text{P}^{-3}$
12. Diantara kelompok molekul dibawah ini yang tidak mengikuti kaidah oktet adalah
A. $\text{CO}_2$, $\text{NH}_3$, $\text{N}_2$
B. $\text{O}_2$, $\text{CO}_3^{-2}$, $\text{CH}_3\text{Cl}$
C. $\text{BCl}_3$, $\text{NO}_2$, $\text{SO}_2$
D. $\text{N}_2\text{O}_4$, HCN, $\text{NH}_4^+$
E. \text{C}_2\text{N}_2$, $\text{ClNO}_2$, $\text{CS}_2$
13. Berikut ini, kelompok mana yang hanya mengandung molekul ikatan kovalen?
A. Al, $\text{O}_3$, $\text{As}_4$
B. $\text{BCl}_3$, $\text{SiCl}_4$, $\text{PCl}_3$
C. $\text{Cl}_2$, NaCl, $\text{H}_2\text{O}$
D. $\text{I}_2$, $\text{H}_2\text{S}$, NaI
E. $\text{NH}_4\text{Br}$, $\text{N}_2\text{H}_4$, HBr
14. Dari senyawa berikut ini, manakah yang kelompok zat mengandung ikatan hidrogen?
A. $\text{NH}_4\text{Cl}(s)$,$\text{NH}_3(l)$ dan $\text{HNO}_3(l)$
B. $\text{NH}_3(l)$, $\text{CH}_3\text{NH}_2(l)$ dan $\text{HNO}_3(l)$
C. $\text{NH}_4\text{Cl}(s)$, $\text{CH}_3\text{NH}_2(l)$ dan $\text{HNO}_3(l)$
D. $\text{NH}_4\text{Cl}(s)$ dan $\text{NH}_3(l)$
E. $\text{NH}_4\text{Cl}(s)$ dan $\text{CH}_3\text{NH}_2(l)$
15. Ikatan apa yang terdapat dalam cis-2-butena berikut ini:
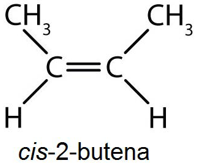

A. 9 ikatan-$\sigma$ dan 3 ikatan-$\pi$
B. 10 ikatan-$\sigma$ dan 2 ikatan-$\pi$
C. 11 ikatan-$\sigma$ dan 1 ikatan-$\pi$
D. 12 ikatan-$\sigma$ dan 1 ikatan-$\pi$
E. 12 ikatan-$\sigma$
16. Untuk reaksi berikut ini:
$2\text{P}(s)+3\text{Cl}_2(g)\to 2\text{PCl}_3(g)$; $\Delta $H = -574 kJ
Berapa mole fosfor yang dibutuhkan untuk menghasilkan panas sebanyak 488 kJ?
$2\text{P}(s)+3\text{Cl}_2(g)\to 2\text{PCl}_3(g)$; $\Delta $H = -574 kJ
Berapa mole fosfor yang dibutuhkan untuk menghasilkan panas sebanyak 488 kJ?
A. 0,85 mole P
B. 1,20 mol P
C. 1,70 mole P
D. 2,35 mol P
E. 3,40 mole P
17. Perhatikan proses reaksi berikut ini:
2 A $\to$ 1/2 B + C; ΔH = 5 kJ/mol
3/2 B + 4 C $\to$ 2 A + C + 3 D; ΔH = -15 kJ/mol
E + 4 A $\to$ C ΔH = 10 kJ/mol
Hitunglah ΔH untuk reaksi : C $\to$ E + 3D
2 A $\to$ 1/2 B + C; ΔH = 5 kJ/mol
3/2 B + 4 C $\to$ 2 A + C + 3 D; ΔH = -15 kJ/mol
E + 4 A $\to$ C ΔH = 10 kJ/mol
Hitunglah ΔH untuk reaksi : C $\to$ E + 3D
A. 0 kJ/mol
B. -20 kJ/mol
C. 10 kJ/mol
D. 20 kJ/mol
E. -10 kJ/mol
18. Zat R dapat bereaksi dapat bereaksi membentuk produk $\text{P}_1$ atau produk $\text{P}_2$. Profil reaksi untuk dua reaksi tersebut ditunjukkan dibawah ini:
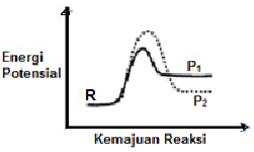
Dibandingkan dengan reaksi $\text{R}\to \text{P}_1$, reaksi $\text{R}\to \text{P}_2$ adalah:

Dibandingkan dengan reaksi $\text{R}\to \text{P}_1$, reaksi $\text{R}\to \text{P}_2$ adalah:
A. Lebih cepat dan kurang endotermis
B. Lebih cepat dan sangat eksotermis
C. Lebih cepat dan lebih endotermis
D. Lebih lambat dan kurang endotermis
E. Lebih lambat dan lebih endotermis
19. Dalam larutan aqueous, ion peroksidisulfat $\text{S}_2\text{O}_8^{-2}$ bereaksi dengan ion iodida sesuai reaksi berikut ini:
$\text{S}_2\text{O}_8^{-2}(aq)+3\text{I}^-$ $\to $ $2\text{SO}_4^{-2}(aq)+\text{I}_3^-(aq)$
Suatu larutan yang disiapkan dengan komposisi 0,050 M ion $\text{S}_2\text{O}_8^{-2}$ dan 0,072 M ion $\text{I}^-$, dan kemajuan reaksi diamati dengan mengukur [$\text{I}^-$]. Diperoleh data seperti pada tabel berikut:

Konsentrasi $\text{S}_2\text{O}_8^{-2}$ yang tersisa pada saat 800 detik adalah
$\text{S}_2\text{O}_8^{-2}(aq)+3\text{I}^-$ $\to $ $2\text{SO}_4^{-2}(aq)+\text{I}_3^-(aq)$
Suatu larutan yang disiapkan dengan komposisi 0,050 M ion $\text{S}_2\text{O}_8^{-2}$ dan 0,072 M ion $\text{I}^-$, dan kemajuan reaksi diamati dengan mengukur [$\text{I}^-$]. Diperoleh data seperti pada tabel berikut:

Konsentrasi $\text{S}_2\text{O}_8^{-2}$ yang tersisa pada saat 800 detik adalah
A. 0,015 M
B. 0,041 M
C. 0,076 M
D. 0,004 M
E. 0,046 M
20. Dua gas diatom, $\text{X}_2$ dan $\text{Y}_2$ bereaksi sesuai persamaan berikut:
$\text{X}_2(g)+\text{Y}_2(g)\rightleftarrows 2\text{XY}(g)$.
Suatu campuran X2 dan Y2 masing masing mengandung 0,5 mol dan dipanaskan dalam wadah tertutup hingga reaksi mencapai kesetimbangan. Grafik berikut ini menunjukkan hubungan antara jumlah mol masing-masing gas dan perubahan waktu.
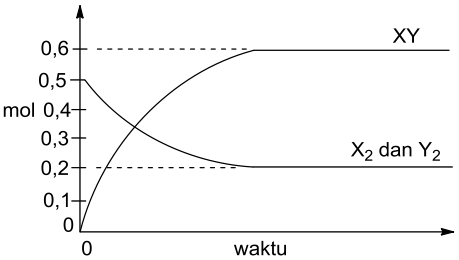
Berdasarkan grafik diatas, berapa nilai konstanta kesetimbangan, $\text{K}_{\text{c}}$, untuk reaksi ini?
$\text{X}_2(g)+\text{Y}_2(g)\rightleftarrows 2\text{XY}(g)$.
Suatu campuran X2 dan Y2 masing masing mengandung 0,5 mol dan dipanaskan dalam wadah tertutup hingga reaksi mencapai kesetimbangan. Grafik berikut ini menunjukkan hubungan antara jumlah mol masing-masing gas dan perubahan waktu.

Berdasarkan grafik diatas, berapa nilai konstanta kesetimbangan, $\text{K}_{\text{c}}$, untuk reaksi ini?
A. 1,5
B. 3
C. 9
D. 12
E. 18
21. Dari reaksi reaksi kesetimbangan dibawah ini, manakah yang pada temperatur konstan bila tekanannya bertambah tidak merubah konsentrasi reaktan dan produk?
A. $\text{N}_2(g)+3\text{H}_2(g)\rightleftarrows 2\text{NH}_3(g)$
B. $2\text{N}_2(g)+\text{O}_2(g)\rightleftarrows 2\text{N}_2\text{O}(g)$
C. $\text{N}_2(g)+2\text{O}_2(g)\rightleftarrows 2\text{NO}_2(g)$
D. $\text{N}_2\text{O}_4(g)\rightleftarrows 2\text{NO}_2(g)$
E. $\text{N}_2(g)+\text{O}_2(g)\rightleftarrows 2\text{NO}(g)$
22. Dalam reaksi:
$\text{CH}_2\text{NH}_2+\text{H}_2\text{PO}_4^{-}\rightleftarrows \text{CH}_3\text{NH}_3^{+}+\text{HPO}_4^{-2}$
Ion $\text{H}_2\text{PO}_4^-$ adalah suatu:
$\text{CH}_2\text{NH}_2+\text{H}_2\text{PO}_4^{-}\rightleftarrows \text{CH}_3\text{NH}_3^{+}+\text{HPO}_4^{-2}$
Ion $\text{H}_2\text{PO}_4^-$ adalah suatu:
A. Asam
B. Basa
C. Agen pengoksidasi
D. Agen pereduksi
E. Katalis
23. Pada $0^\circ \text{C}$, konstanta produk ion dari air, $\text{K}_{\text{w}}=1,2\times 10^{-15}$. Nilai keasaman (pH) dari air murni pada $0^\circ \text{C}$ yaitu:
A. 7,00
B. 6,88
C. 7,56
D. 7,46
E. 7,64
24. Bila 100 mL larutan 0,100 M KOH dicampurkan dengan 100 mL larutan yang mengandung HCl 0,075 M dan asam asetat ($\text{CH}_3\text{COOH}$) 0,050 M maka larutan yang terbentuk mengandung spesi spesi:
A. $\text{K}^+$, $\text{Cl}^-$, $\text{CH}_3\text{COO}^-$, $\text{CH}_3\text{COOH}$
B. $\text{Cl}^-$, $\text{CH}_3\text{COO}^-$, $\text{CH}_3\text{COOH}$, dan $\text{H}^+$
C. $\text{CH}_3\text{COOH}$, $\text{CH}_3\text{COO}^-$, $\text{OH}^-$ dan $\text{H}^+$
D. $\text{K}^+$, $\text{Cl}^-$, $\text{CH}_3\text{COOH}$ dan $\text{H}^+$
E. $\text{K}^+$, $\text{Cl}^-$, $\text{CH}_3\text{COO}^-$, $\text{CH}_3\text{COOH}$, $\text{OH}^-$ dan $\text{H}^+$
25. Sebanyak 100 mL larutan NaOH yang mempunyai pH =12, ditambahkan sebanyak 900 mL air. Nilai pH larutan yang anda peroleh adalah:
A. 1
B. 3
C. 7
D. 11
E. 13
26. Bila anda membuat larutan asam lemah sperti Tabel dibawah ini dengan molaritas yang sama, maka yang akan memberikan pH paling kecil adalah:
A. Asam benzoat ($\text{C}_6\text{H}_5\text{COOH}$); pKa = 4,20
B. Ion benzilammonium ($\text{C}_6\text{H}_5\text{CH}_2\text{NH}_3^+$ ); pKa = 9,35
C. Asam chloroasetat ($\text{ClCH}_2\text{COOH}$); pKa = 2,57
D. Hidroksilamine hidroclorida ($\text{H}_2\text{NOH}\text{.HCl}$); pKa = 5,96
E. Asam Thioasetat ($\text{HSCH}_2\text{COOH}$); pKa = 3,33
27. Apa nama dari senyawa alkena berikut sesuai dengan aturan IUPAC?
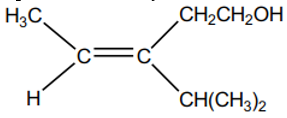

A. trans-3-isopropil-3-pentenol
B. cis-3-isopropil-3-pentenol
C. trans-3-dimetiletana-3-pentenol
D. (Z)-3-isopropil-3-penten-1-ol
E. (E)-3-isopropil-3-pentena-1-ol
28. Reaksi berikut ini:
$\text{CH}_3\text{CHO}+\text{H}_2\text{O}\to \text{CH}_3\text{CH(OH)}_2$
Adalah reaksi:
$\text{CH}_3\text{CHO}+\text{H}_2\text{O}\to \text{CH}_3\text{CH(OH)}_2$
Adalah reaksi:
A. Substitusi
B. Eliminasi
C. Esterifikasi
D. Kondensasi
E. Adisi
29. Dalam kimia organik, kesetabilan suatu senyawa sangat ditentukan oleh adanya substituen. Dari keempat isomer berikut, urutan kestabilan, dari yang paling tidak stabil sampai yang paling stabil, adalah:
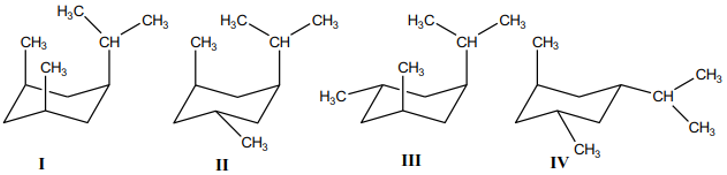

A. I > III , IV > II
B. III , II > IV > I
C. IV > II, III > I
D. IV > I > II , III
E. III, IV > I > II
30. Senyawa alkohol jika dipanaskan dalam suasana asam akan mengalami reaksi dehidrasi menghasilkan akena dengan kerangka yang bebeda dari kerangka senyawa semula, produk utama dari alkena adalah yang sesuai dengan aturan Saytzeff. Manakah produk utama dari alkena yang terjadi di bawah ini?
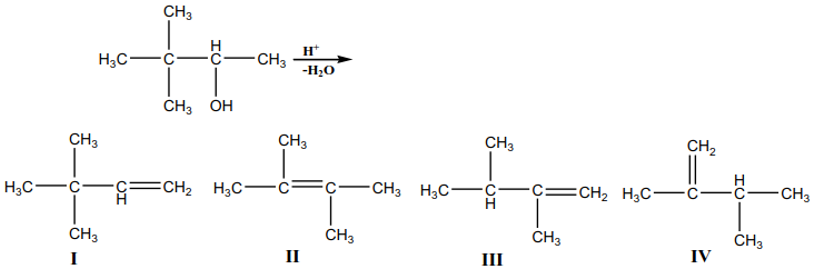

A. Hanya I
B. I dan IV
C. II dan III
D. I dan III
E. Hanya II
This quiz has been created by Ayo Berlatih
