Soal Olimpiade Kimia OSN-K SMA 2015

AYO BERLATIH
Soal Olimpiade Kimia OSN-K SMA 2015
| Nama Peserta | : | |
| Tanggal Test | : | |
| Jumlah Soal | : | 25 soal |
| Waktu | : | 90 menit |
Pilihlah Jawaban yang tepat.
1. Hasil analisis senyawa berupa gas menunjukkan kandungan (% massa) 33,0% Si dan 67,0% F. Pada temperatur $35^\circ \text{C}$, sebanyak 0,210 L senyawa tersebut memberikan tekanan 1,70 atm. Jika massa 0,210 L senyawa tersebut adalah 2,40 g, maka rumus molekulnya adalah:
A. $\text{SiF}_4$
B. $\text{SiF}_3$
C. $\text{Si}_2\text{F}_8$
D. $\text{Si}_2\text{F}_6$
E. $\text{Si}_3\text{F}_9$
2. Dari persamaan reaksi berikut ini, yang merupakan reaksi oksidasi-reduksi adalah:
A. $2HCl(aq)+Mg(s)\to MgCl_2(aq)+H_2(g)$
B. $Na_2O(s)+H_2O(l)\to 2NaOH(aq)$
C. $CO_2(g)+H_2O(l)\to H_2CO_3(aq)$
D. $CaO(s)+SO_3(g)\to CaSO_4(s)$
E. $NH_3(g)+HCl(g)\to NH_4Cl(s)$
3. Konsentrasi (dalam satuan molalitas) senyawa para-diklorobenzena ($C_6H_4Cl_2$) dalam suatu larutan yang dibuat dengan cara melarutkan 2,65 g $C_6H_4Cl_2$ dalam 50 mL benzena (densitas = 0,879 g/mL) adalah:
A. 0,018 m
B. 0,041 m
C. 0,180 m
D. 0,410 m
E. 1,810 m
4. Titanium(IV)oksida secara luas digunakan dalam industri cat sebagai pigmen putih. Senyawa ini larut dalam asam sulfat pekat panas sesuai persamaan reaksi berikut,
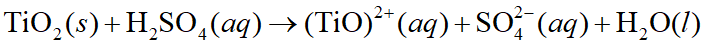
Pernyataan yang tepat untuk menyatakan jenis reaksi tersebut adalah:
Pernyataan yang tepat untuk menyatakan jenis reaksi tersebut adalah:
A. Asam-basa
B. pembentukan ion kompleks
C. dehidrasi
D. pertukaran
E. redoks
5. Di antara pernyataan berikut yang benar adalah:
A. $^{18}\text{O}$ dan $^{19}\text{F}$ mempunyai jumlah neutron sama.
B. $^{14}\text{C}$ dan $^{14}\text{N}$ adalah isotop karena nomor massanya sama.
C. $^{18}\text{O}^{-2}$ mempunyai jumlah elektron yang sama dengan 20Ne.
D. A dan B benar.
E. A dan C benar.
6. Dari serangkaian diagram berikut ini, diagram yang terbaik untuk menjelaskan jari-jari relatif dari atom dan ion natrium serta atom klor dan ion klorida adalah:
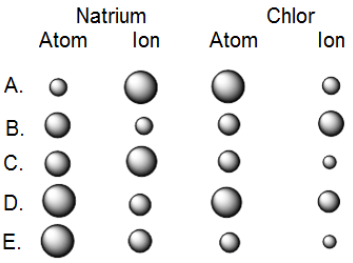

A
B
C
D
E
7. Energi ionisasi kedua kalsium adalah 1150 kJ.mol-1. Di antara persamaan reaksi termokimia berikut yang menggambarkan energi ionisasi kedua kalsium adalah:
A. $Ca(g)\to Ca^{2+}(g)+2e^-$; $\Delta \text{H}^\circ $ = +1150 kJ/mol.
B. $Ca^+(g)\to Ca^{2+}(g)+e^-$; $\Delta \text{H}^\circ $ = +1150 kJ/mol.
C. $Ca^+(g)\to Ca^{2+}(g)+e^-$; $\Delta \text{H}^\circ $ = -1150 kJ/mol.
D. $Ca(s)\to Ca^{2+}(g)+2e^-$; $\Delta \text{H}^\circ $ = +1150 kJ/mol.
E. $Ca^+(s)\to Ca^{2+}(g)+e^-$; $\Delta \text{H}^\circ $ = -1150 kJ/mol.
8. Diagram berikut ini menggambarkan suatu percobaan untuk pembuatan dan pengumpulan gas $\text{SO}_2$. Ternyata setelah dilakukan percobaan, percobaan dengan sistem tersebut gagal (tidak dapat mengumpulkan gas $\text{SO}_2$).
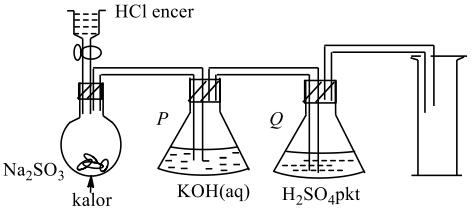
Di antara modifikasi berikut yang akan membuat eksperimen ini berhasil untuk memperoleh gas $\text{SO}_2$ adalah:

Di antara modifikasi berikut yang akan membuat eksperimen ini berhasil untuk memperoleh gas $\text{SO}_2$ adalah:
A. Menghilangkan labu P seluruhnya
B. Menghilangkan labu Q seluruhnya
C. Memakai asam sulfat encer pengganti asam hidroklorida
D. Memakai air dalam labu P pengganti akua kalium hidroksida
E. Pengumpulan dengan cara pemindahan ke atas
9. Anda mempunyai zat berikut ini:
i. Kristal garam NaCl
ii. Lelehan garam NaCl
iii. Larutan garam NaCl
Yang dapat menghantarkan listrik adalah:
i. Kristal garam NaCl
ii. Lelehan garam NaCl
iii. Larutan garam NaCl
Yang dapat menghantarkan listrik adalah:
A. i dan ii
B. i dan iii
C. ii dan iii
D. i, ii, dan iii
E. hanya iii
10. Yang merupakan diagram orbital hibrida dari boron dalam $\text{BF}_3$ adalah:
A. 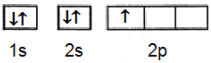

B. 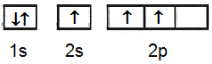

C. 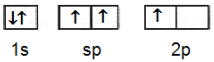

D. 

E. 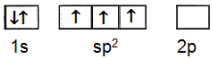

11. Dalam molekul 1-butena, atom karbon yang diberi label 1 mempunyai hibridisasi
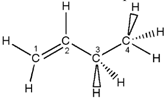

A. $\text{sp}^2$
B. $\text{sp}^3$
C. $\text{sp}^4$
D. sp
E. $\text{sp}^3\text{d}$
12. Di antara pasangan molekul berikut yang mempunyai geometri sama adalah:
A. $\text{AlCl}_3$ dan $\text{BCl}_3$
B. $\text{AlCl}_3$ dan $\text{PCl}_3$
C. $\text{BF}_3$ dan $\text{NH}_3$
D. $\text{BeCl}_2$ dan $\text{H}_2\text{O}$
E. $\text{CO}_2$ dan $\text{SO}_2$
13. Di antara molekul atau ion berikut: $\text{SO}_2$, $\text{CO}_2$, $\text{NO}_2^+$, $\text{ClO}_2^-$, molekul atau ion yang isoelektronik adalah:
A. $\text{SO}_2$, $\text{NO}_2^+$, dan $\text{ClO}_2^-$
B. $\text{SO}_2$ dan $\text{CO}_2$
C. $\text{SO}_2$ dan $\text{NO}_2^+$
D. $\text{CO}_2$ dan $\text{ClO}_2^-$
E. $\text{CO}_2$dan $\text{NO}_2^+$
14. Satu dari struktur resonansi ion $\text{OCN}-$ yang digambarkan di bawah ini
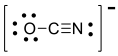
Muatan formal untuk setiap atom dalam struktur resonansi di atas adalah:
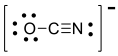
Muatan formal untuk setiap atom dalam struktur resonansi di atas adalah:
A. atom O = –1, atom C atom = –1, dan atom N = +1
B. atom O = 0, atom C = 0, dan atom N = –1
C. atom O = –1, C atom = 0, dan atom N = 0
D. atom O = 0, C atom = 0, dan atom N = 0
E. atom O = +1, atom C = 0, dan atom N = –2
15. Persamaan reaksi kimia yang menunjukkan hubungan Kp = Kc adalah:
A. $\text{MgCO}_3(s)+2\text{HCl}(g)$ $\rightleftharpoons $ $\text{MgCl}_2(s)+\text{CO}_2(g)+\text{H}_2\text{O}(l)$
B. $\text{C}(s)+\text{O}_2(g)$ $\rightleftharpoons $ $\text{CO}_2(g)$
C. $\text{CH}_4(g)+2\text{O}_2(g)$ $\rightleftharpoons $$\text{CO}_2(g)+2\text{H}_2\text{O}(l)$
D. $\text{Zn}(s)+2\text{HCl}(aq)$ $\rightleftharpoons $ $\text{H}_2(g)+\text{ZnCl}_2(aq)$
E. $2\text{N}_2(g)+5\text{O}_2(g)$ $\rightleftharpoons $ $2\text{N}_2\text{O}_5(g)$
16. Dalam suatu wadah tertutup yang suhunya 25$^\circ C$, sejumlah ammonium karbamat ($\text{N}_2\text{H}_6\text{CO}_2$) menyublim dan terdisosiasi menjadi ammoniak $(NH_3)$ serta karbondioksida ($\text{CO}_2$) sesuai persamaan reaksi berikut:
$\text{N}_2\text{H}_6\text{CO}_2(s)\to 2\text{NH}_3(g)+\text{CO}_2(g)$
Setelah didiamkan beberapa lama, terjadi kesetimbangan dengan tekanan total gas sebesar 0,116 atm. Nilai Kp untuk reaksi tersebut adalah:
$\text{N}_2\text{H}_6\text{CO}_2(s)\to 2\text{NH}_3(g)+\text{CO}_2(g)$
Setelah didiamkan beberapa lama, terjadi kesetimbangan dengan tekanan total gas sebesar 0,116 atm. Nilai Kp untuk reaksi tersebut adalah:
A. 4,20 x $10^{-3}$
B. 2,99 x $10^{-3}$
C. 4, 64 x $10^{-4}$
D. 3,40 x $10^{-4}$
E. 2,31 x $10^{-4}$
17. Larutan garam-garam di bawah ini masing-masing konsentrasinya adalah 0,1 M. Larutan yang memiliki nilai pH paling tinggi adalah:
A. Larutan $\text{NH}_4\text{Cl}$ (Kb $\text{NH}_4\text{OH}$ = 2,0 x $10^{-5}$)
B. Larutan $(\text{NH}_4)_2\text{SO}_4$ (Kb $\text{NH}_4\text{OH}$ = 2,0 x $10^{-5}$)
C. Larutan NaClO (Ka HClO = 3,4 x $10^{-8}$)
D. Larutan NaCN (Ka HCN = 4,0 x $10^{-10}$)
E. Larutan $\text{Na}_2\text{S}$ (Ka $\text{H}_2\text{S}$ = 1,3 x $10^{-20}$)
18. Dalam fotografi, padatan AgBr yang tersisa dilarutkan dalam larutan $\text{Na}_2\text{S}_2\text{O}_3$. Ion $\text{Ag}^+$ bereaksi dengan ion $\text{S}_2\text{O}_3^{2-}$ membentuk senyawa kompleks $[\text{AgS}_2\text{O}_3)_2]^{3-}$, dengan persamaan reaksi sebagai berikut:
$\text{AgBr}(s)\rightleftharpoons \text{Ag}^+(aq)+\text{Br}^{-}(aq)$; $\text{K}_{\text{sp}}=5,4\times 10^{-13}$
$\text{Ag}^+(aq)+2\text{S}_2\text{O}_3^{2-}(aq)$ $\rightleftharpoons $ $[\text{Ag}\left( \text{S}_2\text{O}_3 \right)_2]^{3-}(aq)$; $\text{K}_{\text{f}}=2,0\times 10^{13}$
Jumlah padatan AgBr yang dapat larut dalam 125 mL larutan Na2S2O3 1,20 M adalah:
$\text{AgBr}(s)\rightleftharpoons \text{Ag}^+(aq)+\text{Br}^{-}(aq)$; $\text{K}_{\text{sp}}=5,4\times 10^{-13}$
$\text{Ag}^+(aq)+2\text{S}_2\text{O}_3^{2-}(aq)$ $\rightleftharpoons $ $[\text{Ag}\left( \text{S}_2\text{O}_3 \right)_2]^{3-}(aq)$; $\text{K}_{\text{f}}=2,0\times 10^{13}$
Jumlah padatan AgBr yang dapat larut dalam 125 mL larutan Na2S2O3 1,20 M adalah:
A. 7,14 g
B. 12,22 g
C. 14,08 g
D. 16,72 g
E. 40,65 g
19. Percobaan yang melibatkan reaksi oksidasi NO menjadi NO2 berlangsung sesuai persamaan reaksi berikut:
$2\text{NO}(g)+\text{O}_2(g)\to \text{NO}_2(g)$
Data yang diperoleh dari percobaan tersebut adalah sebagai berikut:
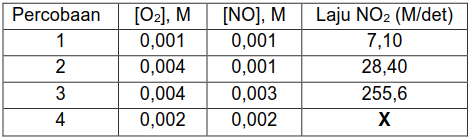
Nilai X dalam tabel adalah:
$2\text{NO}(g)+\text{O}_2(g)\to \text{NO}_2(g)$
Data yang diperoleh dari percobaan tersebut adalah sebagai berikut:

Nilai X dalam tabel adalah:
A. 3,65
B. 14,20
C. 28,40
D. 56,80
E. 85,20
20. Di dalam reaksi yang digambarkan oleh persamaan reaksi berikut ini:
$C_6H_6+Cl_2\to C_6H_5Cl+HCl$
Jenis reaksi yang terjadi pada benzena adalah:
$C_6H_6+Cl_2\to C_6H_5Cl+HCl$
Jenis reaksi yang terjadi pada benzena adalah:
A. Addisi elektrofilik
B. Substitusi elektrofilik
C. Substitusi radikal bebas
D. Addisi nukleofilik
E. Substitusi nukleofilik
21. Aldehida dan keton dihasilkan secara industri oleh katalitik oksidasi alkena, seperti etanal dibuat di industri petrokimia dari etena seperti persamaan reaksi berikut:
$\text{H}_2\text{C}=\text{CH}_2+\tfrac{1}{2}\text{O}_2\text{---katalis}\to \text{CH}_3\text{CHO}$
Proses ini juga dipakai di industri untuk membuat 2-butena. Yang menggambarkan struktur senyawa yang dapat dihasilkan 2-butena adalah:
$\text{H}_2\text{C}=\text{CH}_2+\tfrac{1}{2}\text{O}_2\text{---katalis}\to \text{CH}_3\text{CHO}$
Proses ini juga dipakai di industri untuk membuat 2-butena. Yang menggambarkan struktur senyawa yang dapat dihasilkan 2-butena adalah:
A. $\text{CH}_3\text{CH}_2\text{CHO}$
B. $\text{CH}_3\text{CH}_2\text{CH}_2\text{CHO}$
C. $\text{CH}_3\text{COCH}_2\text{CH}_3$
D. $\text{CH}_3\text{COCH}_3$
E. $(\text{CH}_3)_2\text{CHCHO}$
22. Di antara senyawa berikut yang dapat dibuat dari reaksi antara bromoetana dengan kalium sianida dan kemudian produk yang terbentuk direduksi lebih lanjut, adalah:
A. $\text{CH}_3\text{CH}_3$
B. $\text{CH}_3\text{CH}_2\text{NH}_2$
C. $\text{CH}_3\text{CH}_2\text{CH}_3$
D. $\text{CH}_3\text{CH}_2\text{CH}_2\text{NH}_2$
E. $\text{CH}_3\text{CH_2}\text{CH}_2\text{CH}_2\text{NH}_2$
23. Produk yang akan terbentuk jika propenaldehida dioksidasi dengan KMnO4 pada suhu ruang adalah:
A. $\text{CH}_2\text{(OH)CH(OH)COOH}$
B. $\text{CH}_2\text{(OH)CH(OH)COH}$
C. $\text{CH}_2=\text{C(OH)COOH}$
D. $\text{CH}_2=\text{CHCOOH}$
E. $\text{CH}_3\text{CO}+\text{CO}_2$
24. Produk yang akan dihasilkan jika 3-metil-1-pentena direaksikan dengan $\text{Cl}_2$ dengan adanya sinar UV adalah:
A. 5-kloro-3-metil-1-pentena
B. 4-kloro-3-metil-1-pentena
C. 3-kloro-3-metil-1-pentena
D. 1,2-dikloro-3-metilpentana
E. 1-kloro-3-metilpentana
25. Senyawa ester P yang berbau buah-buahan mempunyai struktur seperti berikut:
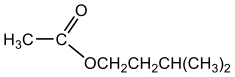
Senyawa yang dihasilkan jika P dihidrolisis dengan asam hidroklorida adalah
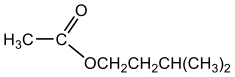
Senyawa yang dihasilkan jika P dihidrolisis dengan asam hidroklorida adalah
A. $\text{CH}_3\text{COCl}$ dan $(\text{CH}_3)_2\text{CHCH}_2\text{CH}_2\text{OH}$
B. $\text{CH}_3\text{CHO}$ dan $(\text{CH3})2\text{CHCH}_2\text{CH}_2\text{OH}$
C. $\text{CH}_3\text{CO}_2\text{H}$ dan $(\text{CH}_3)_2\text{CHCH}_2\text{CHO}$
D. $\text{CH}_3\text{CO}_2\text{H}$ dan $(\text{CH}_3)_2\text{CHCH}_2\text{CH}_2\text{OH}$
E. $\text{CH}_3\text{CH}_2\text{CO}_2\text{H}$ dan $(\text{CH}_3)_2\text{CHCH}_2\text{CHO}$
This quiz has been created by Ayo Berlatih
